Além do fosfato de lítio (pó branco), a técnica gera hidrogênio e cloro, que cobrem os custos de eletricidade do processo de mineração.
Mineração oceânica
Existe cerca de 5.000 vezes mais lítio nos oceanos do que na terra, o que tem levado engenheiros e cientistas a tentarem fabricar baterias que funcionem com água do mar ou desenvolver técnicas para a mineração oceânica do metal, cada vez mais escasso e mais caro.
O problema é que, na água do mar, o lítio está presente em concentrações extremamente baixas, de cerca de 0,2 parte por milhão (ppm).
Íons maiores, como sódio, magnésio e potássio, estão todos presentes na água do mar em concentrações muito mais altas, mas, apesar dos esforços, até agora ninguém havia conseguido extrair o lítio dessa mistura de forma técnica ou economicamente viável.
Esse desafio acaba de ser vencido por Zhen Li e colegas da Universidade de Ciência e Tecnologia Rei Abdullah, na Arábia Saudita.
Extração de lítio da água do mar
A equipe desenvolveu uma célula eletroquímica contendo uma membrana cerâmica feita de óxido de lítio e uma liga lantânio-titânio, uma mistura conhecida como LLTO (lítio-lantânio-titânio-oxigênio).
A estrutura cristalina dessa cerâmica contém orifícios largos o suficiente para permitir a passagem dos íons de lítio, mas não dos íons de metal maiores, bloqueando efetivamente sódio, magnésio, potássio e outros.
A célula eletroquímica contém três compartimentos. A água do mar flui para uma câmara de alimentação central, onde os íons de lítio positivos passam através da membrana LLTO até um compartimento lateral, que contém uma solução de armazenamento temporário e um catodo de cobre revestido com platina e rutênio. Enquanto isso, os íons negativos saem da câmara de alimentação através de uma membrana de troca aniônica padrão, passando para um terceiro compartimento contendo uma solução de cloreto de sódio e um anodo igualmente de platina e rutênio.
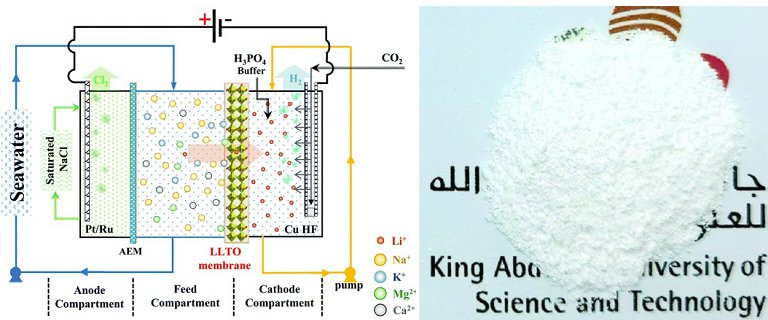
[Imagem: Zhen Li et al. – 10.1039/D1EE00354B]
Fosfato de lítio e subprodutos valiosos
O reator de extração de lítio foi testado usando água do Mar Vermelho. A uma tensão de 3,25 V, a célula gera gás hidrogênio no catodo e gás cloro no anodo. Isso impulsiona o transporte do lítio através da membrana LLTO, para se acumular na câmara lateral.
Essa água enriquecida com lítio – a solução de armazenamento temporário – torna-se então a matéria-prima para mais quatro ciclos de processamento, até que a solução atinja uma concentração de mais de 9.000 ppm.
O produto final é fosfato de lítio sólido, contendo apenas traços de outros íons metálicos, o que é puro o suficiente para atender aos requisitos dos fabricantes de baterias.
Os pesquisadores estimam que a célula precisaria de apenas US$ 5 de eletricidade para extrair 1 quilograma de lítio da água do mar. O valor do hidrogênio e do cloro produzidos pela célula mais do que compensaria esse custo, e a água do mar residual também poderia ser usada em usinas de dessalinização para fornecer água doce, uma vez que a maior parte dos sais já teria sido retirada.
“Continuaremos otimizando a estrutura da membrana e o projeto da célula para melhorar a eficiência do processo,” disse o professor Zhiping Lai, coordenador da equipe, acrescentando que está buscando colaboração da indústria de vidros para produzir a membrana LLTO em grande escala e a um custo acessível.
Outra modificação bem-vinda seria a substituição dos catalisadores de platina e rutênio, que são metais raros e caros.
Fonte: Inovação Tecnológica



